Забрюшинные опухоли
Жалобы и анамнез
- наличие пальпируемого опухолевого образования в животе;
- боли в животе – от тупых, ноющих незначительных болей до сильных, приступообразных;
- желудочный дискомфорт – потеря аппетита, отрыжка, иногда рвота, чувство тяжести в верхней половине живота;
- кишечные расстройства – запоры, поносы, чередование запоров с поносами, урчание и вздутие живота;
- нарушение общего состояния больного – общее недомогание, повышенная утомляемость, слабость, похудание, лихорадка, бледность кожных покровов;
- наличие пальпируемой опухоли.
Очень важно! Типичным признаком забрюшинных опухолей является отсутствие специфических симптомов. Клиническая картина заболевания обусловлена не видом новообразования, а его локализацией, близостью тех или иных органов и анатомических образований (кровеносных сосудов, нервов, лимфатических протоков) и их прорастанием.
Физикальное обследование:
Данные объективного исследования:
- осмотр: бледность кожных покровов, ассиметрия живота;
- пальпация живота: пальпаторное обнаружение опухоли, зависит от стадии заболевания, анатомической формы роста, напряжения брюшной стенки;
- перкуссия живота: притупление над опухолью.
Лабораторные исследования:
- общий анализ крови – характерны гипохромная анемия, повышение СОЭ, лейкоцитоз;
- анализ кала на скрытую кровь – положительная реакция при прорастании опухолью толстой кишки;
- коагулограмма – наблюдаются признаки гиперкоагуляции;
- анализ крови на онкомаркеры: АФП, РЭА – повышаются (не всегда).
Инструментальные исследования:
- УЗИ органов брюшной полости и забрюшинного пространства – с целью уточнения распространенности опухолевого процесса, прорастания опухоли в соседние органы и структуры, выявления отдаленных метастазов в печени и забрюшинных лимфоузлах;
- КТ/МРТ – с целью уточнения распространенности опухолевого процесса, прорастания опухоли в соседние органы и структуры, выявления отдаленных метастазов в печени и забрюшинных лимфоузлах;
- рентгеногафия грудной клетки в двух проекциях, при необходимости рентгеновская томография, компьютерная томография – для выявления метастазов в легких (по показаниям);
- ПЭТ – один из наиболее чувствительных и информативных методов выявления «маленьких» опухолей, рецидивов, микрометастазов.
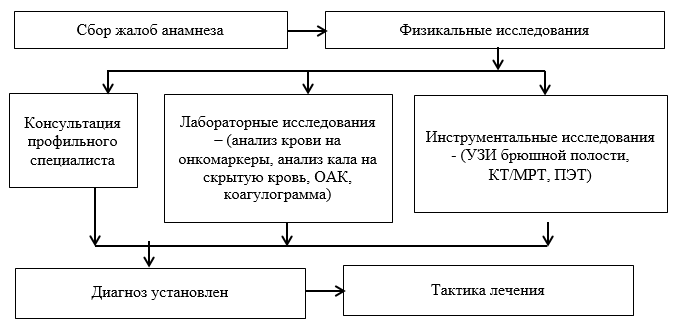
Диагностический алгоритм:
Дифференциальный диагноз и обоснование дополнительных исследований:
Внеорганные забрюшинные опухоли дифференцируют опухолями, с кистами почек и яичников. Применяемые в настоящее время специальные методы исследования дают возможность у большинства больных правильно поставить диагноз.
Необходимо помнить и о новообразованиях мочеточников, хотя они встречаются крайне редко. Ошибки в дифференциальной диагностике забрюшинных новообразований и опухолей желудочно-кишечного тракта встречаются реже и, как правило, обусловлены недостаточным обследованием больного или неправильной трактовкой рентгенологических данных.
К числу заболеваний, которые могут симулировать внеорганные забрюшинные опухоли, относится также аневризма брюшной аорты и ее ветвей.
Забрюшинные лимфатические узлы являются зоной как регионарных, так и отдаленных метастазов из опухолей различных органов. Возможность вторичных новообразований в этой области следует учитывать при дифференциальной диагностике забрюшинных опухолей. Кроме перечисленных выше опухолей, забрюшинно могут локализоваться неспецифические и специфические воспалительные процессы, паразитарные кисты, гематомы.
Диагноз Обоснование для дифференциальной диагностики Обследования Критерии исключения диагноза
Кисты почек и яичников Киста почки — патологическое состояние, при котором происходит аномальное разрастание полого образования. Размеры полосного образования могут быть мелкие от 1 см, до больших — 10 см в диаметре, быть единичными или множественными.
Киста яичника – это заполненное жидкостью выпячивание, образующееся на поверхности одного или обоих яичников женщин в большинстве случаев из фолликула. Анатомически киста выглядит как тонкостенная полость в виде мешочка. Размеры этого образования колеблются от нескольких до 15-20 сантиметров в диаметре.
В 90 % случаев киста является функциональной, или фолликулярной. УЗИ ОБП и ЗП, МРТ ОБП и ЗП, КТ ОБП и ЗП, лапароскопия. Наличие внутритканевой кисты
Аневризма аорты и ее ветвей Аневризма аорты – патологическое локальное расширение участка магистральной артерии, обусловленное слабостью ее стенок. В зависимости от локализации аневризма аорты может проявляться болью в грудной клетке или животе, наличием пульсирующего опухолевидного образования, симптомами компрессии соседних органов: одышкой, кашлем, дисфонией, дисфагией, отечностью и цианозом лица и шеи. Рентгенография грудной клетки и брюшной полости, аортография) и ультразвуковые методы (УЗДГ, УЗДС грудной/брюшной аорты). Выявленные аневризматические сосуда
Гематомы Забрюшинные гематомы - образуются чаще всего при переломах костей таза (46,9%), забрюшинно расположенных органов (31,6%), повреждениях позвоночника (21,5%). Как правило, забрюшинные кровоизлияния встречаются при наиболее тяжелых видах травмы у больных с сочетанными повреждениями. УЗИ ОБП и ЗП, МРТ ОБП и ЗП, КТ ОБП и ЗП. Наличие предшествующей травмы и обьемного образования забрюшинного образования.
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ
Тактика лечения:
- ликвидация опухолевого очага и метастазов;
- достижение полной или частичной регрессии, стабилизации опухолевого процесса.
Тактика лечения:
- Стадия Ia (Т1b N0, NX M0, низкая степень злокачественности): хирургическое удаление опухоли.
- Стадия Ib (Т2b N0, NX M0, низкая степень злокачественности): хирургическое удаление опухоли + послеоперационная лучевая терапия на область резидуальной опухоли в СОД 60–70 Гр, РОД 2 Гр (при R1, R2).
- Стадии II–III (Т1b–Т2b N0, N1 M0, высокая степень злокачественности): хирургическое удаление опухоли (при N+ выполняется лимфодиссекция) + послеоперационная лучевая терапия (СОД 40–50 Гр, РОД 2 Гр) + 3–4 курса адъюванной химиотерапии (при чувствительных гистологических типах опухоли).
При R1, R2 суммарная очаговая доза лучевой терапии на область ре-
зидуальной опухоли должна быть увеличена до 60–70 Гр (без превышения толерантных доз на здоровые органы и ткани).
При сомнении в резектабельности или нерезектабельной опухоли проводится курс лучевой терапии в СОД 40–50 Гр в режиме классического фракционирования и/или 2–3 курса химиотерапии (предпочтительнее в условиях общей или регионарной гипертермии).
При сохранении нерезектабельности опухоли проводится лучевая терапия
до СОД 60–70 Гр за весь курс лечения ± 3–4 курса химиотерапии (схема лечения
определяется исходя из оценки эффективности неоадъювантной химиотерапии по данным компьютерной томографии или ультразвукового исследования).
- Стадия IV (любая Т и N M1, любая степень злокачественности):
паллиативное лечение по индивидуальным программам с включением химиотерапии и/или лучевой терапии, в том числе в модифицированных условиях (общая и регионарная гипертермия);
хирургические вмешательства для уменьшения опухолевой массы и ликвидации симптомов опухолевой компрессии. Резекция отдаленных метастазов оправдана при контролируемом опухолевом процессе.
NB! при резектабельной опухоли и наличии одиночных и единичных метастазов в отдаленных органах – циторедуктивная операция с одномоментным или отсроченным удалением метастазов.
Критерии резектабельности метастазов в печени – отсутствие нерезектабельных экстрапеченочных метастазов, функциональная переносимость и отсутствие сопутствующих заболеваний в стадии суб – и декомпенсации), возможность удаления всех метастазов с клиренсом не менее 0,1 см без опухолевого роста и поражение менее 70% или 6 сегментов печени.
Критерии эффективности лечения:
- полный эффект – исчезновение всех очагов поражения на срок не менее 4-х недель;
- частичный эффект – большее или равное 50% уменьшение всех или отдельных опухолей при отсутствии прогрессирования других очагов;
- стабилизация – (без изменений) уменьшение менее чем на 50% или увеличение менее чем на 25% при отсутствии новых очагов поражения;
- прогрессирование – увеличение размеров одной или более опухолей более 25% либо появление новых очагов поражения
Немедикаментозное лечение
- Режим – больного при проведении консервативного лечения – общий. В ранний послеоперационный период – постельный или полупостельный (в зависимости от объема операции и сопутствующей патологии). В послеоперационном периоде – палатный.
- Диета – Стол №1 после хирургического лечения, затем переход на Стол №2.
- Лучевая терапия:
Послеоперационная лучевая терапия показана при степени местного распространения соответствующей St Ib – St IV.
Проводится послеоперационная лучевая терапия на область резидуальной опухоли в СОД 60–70 Гр, РОД 2 Гр (при R1, R2).
При сомнении в резектабельности или нерезектабельной опухоли проводится курс лучевой терапии в СОД 40–50 Гр в режиме классического фракционирования.
Лучевая терапия проводится в конвенциальном (стандартном) или конформном режиме облучения в статическом многопольном режиме РОД 2-2,5-3,0 Гр до СОД 40–60Гр на зону врастания опухоли. При проведении лучевой терапии возможно применение препаратов, защищающих организм от лучевого повреждения.
Облучение проводят на гамма-терапевтических аппаратах или линейных ускорителях.
Медикаментозное лечение
Химиотерапия нейроэндокринных опухолей:
Химиотерапия назначается при невозможности хирургического лечения, после циторедуктивных операций.
Функционирующие НЭО G1-G3: аналоги соматостатина (симптоматическая терапия):
Октреотид 0,1 мг п/к, 3 раза в сутки в течение короткого периода времени (примерно 2 недели) с целью оценки его эффективности и общей переносимости
затем
Октреотид ЛАР 20 мг внутримышечно 1 раз в 28 дней.
Если в течение 3 месяцев обеспечивается адекватный контроль клинических проявлений и биологических маркеров заболевания – октреотид ЛАР 10 мг, внутримышечно 1 раз/28 дней.
Если в течение 3 месяцев обеспечивается только частичный контроль клинических проявлений и биологических маркеров заболевания – октреотид ЛАР 30 мг внутримышечно каждые 4 недели.
Распространенные нейроэндокринные опухоли толстой кишки или с неизвестной локализацией первичной опухоли – октреотид ЛАР 30 мг внутримышечно 1раз/28 дней до прогрессирования.
Нефункционирующие НЭО:
Ki67<2-10%, G1/G2:
- аналоги соматостатина;
- α-ИФН;
- эверолимус 10мг внутрь ежедневно до прогрессирования;
- эверолимус 10мг внутрь ежедневно в комбинации с октреотид ЛАР 1раз/28 дней, до прогрессирования
Ki67 3-20%, G1/G2:
- фторурацил+эверолимус;
- темозоломид+капецитабин;
- аналоги соматостатина.
Ki67>20%, G3:
- карбоплатин/цисплатин+этопозид;
- темозоломид+бевацизумаб;
- аналоги соматостатина.
Практические рекомендации по лекарственному лечению гастроинтестинальных стромальных опухолей (GIST)
Лечение нерезектабельных опухолей при рецидиве или метастатической болезни
Терапия первой линии:
При нерезектабельных опухолях, рецидиве или метастатической болезни основной метод лечения – таргетная терапия иматинибом 400 мг в сутки. При выявлении мутации в 9-м экзоне гена KIT рекомендован иматиниб 800 мг в сутки (достоверно увеличивает время до прогрессирования без статистически значимого улучшения общей выживаемости). При прогрессировании на фоне приема иматиниба в дозе 400 мг в сутки показана эскалация дозы до 800 мг в сутки. При исходно нерезектабельных опухолях у больных с эффектом в результате терапии целесообразна оценка возможности радикального хирургического лечения через 6–12 месяцев после начала терапии.
Терапия второй линии:
При прогрессировании заболевания на фоне приема иматиниба (после эскалации дозы с 400 до 800 мг), непереносимости иматиниба либо первичной резистентности показана терапия сунитинибом: 50 мг в сутки, 4 недели с двухнедельным перерывом. При выраженных побочных эффектах допустимо снижение дозы до 37,5 мг в сутки.
Саркомы мягких тканей
Распространенный опухолевый процесс – стадия III–IV:
Химиотерапия является основным методом лечения диссеминированного процесса при мягкотканых саркомах. Наиболее часто используются доксорубицин, ифосфамид, дакарбазин. Стандартом химиотерапии диссеминированных сарком мягких тканей первой линии является комбинированный режим доксорубицин + ифосфамид. Для пациентов старше 65 лет методом выбора является монотерапия антрациклинами. При общем хорошем состоянии комбинированная химиотерапия предпочтительнее, когда ожидается выраженный эффект со стороны опухоли. При поверхностных ангиосаркомах альтернативой является назначение таксанов, показавших высокую противоопухолевую активность при данном гистологическом типе. Паклитаксел показал высокую эффективность в терапии местнораспространенных ангиосарком, в частности ассоциированных с синдромом Стюарта-Тривса.
В качестве >2 линии в лечении липосарком, лейомиосарком, синовиальной и экстраоссальной формы саркомы Юинга может быть использован трабектедин. Также во вторую и более линии для большинства гистологических подтипов, за исключением липосарком и GIST, может быть использован пазопаниб. Для липосарком возможно использование эрибулина. Гемцитабин показал наличие противоопухолевой активности в качестве единственного противоопухолевого агента и при лейомиосаркоме. Дакарбазин, назначенный в качестве второй линии химиотерапии, также обладает некоторой противоопухолевой активностью (вероятно, более всего в лечении лейомиосаркомы. Пазопаниб используется в качестве второй и более линий для лечения большинства гистологических подтипов, однако для химиорезистентных гистотипов (альвеолярная саркома мягких тканей, светлоклеточная саркома мягких тканей, солитарная фиброзная опухоль/гемангиоэндотелиома) должен применяться в первую линию лечения.
Наблюдение у больных, закончившим этап комбинированного лечения, динамическое наблюдение проводится каждые 3 месяца в течение первых 2 лет, далее раз в 6 месяцев до 5 лет.
